FDA-Anforderungen - FEM-Analyse von einteiligen Keramikimplantaten gemäß EN ISO 14801
In-silico-Simulationsmethoden haben das Potenzial, die Zulassung von Medizinprodukten zu revolutionieren, indem sie In-vitro- und In-vivo-Tests zuverlässig ersetzen. Durch den Wechsel zum virtuellen Patienten ergeben sich für Medizinproduktehersteller zahlreiche Vorteile: frühzeitiges Eingreifen in die Produktentwicklung, sicheres Testen und Anpassen, Vermeidung von zeit- und kostenintensiven Human- und Tierversuchen. Das innovative Schweizer Unternehmen SDS profitiert bereits von den Möglichkeiten der FEM-Analyse im Zulassungsverfahren.

„Die FEM-Analyse von Simq ermöglichte es uns, die Anfragen der FDA in einem kritischen Zulassungsschritt für unser Produkt schnell zu beantworten und eine reibungslose Produkteinführung in den USA zu gewährleisten“.
Dr. Karl Ulrich Volz / CEO / SDS Swiss Dental Solutions
Dr. Karl Ulrich Volz / CEO / SDS Swiss Dental Solutions
Über unseren Kunden
Gegründet vom Keramikpionier und Implantologen Dr. Ulrich Volz, bietet Swiss Dental Solutions ein umfassendes Behandlungskonzept für biomedizinische Implantatlösungen mit Keramikimplantaten.

Antwort auf eine FDA-Anfrage: Die U.S. Food and Drug Administration (FDA) forderte den Nachweis, dass weitere Varianten der von SDS – Swiss Dental Solution bereits erfolgreich in einem physikalischen Ermüdungstest getesteten Keramikimplantate keine höheren Belastungen aufweisen. Die Antwort auf diese FDA-Anforderung musste innerhalb von 120 Tagen erfolgen. Eine erneute physikalische Prüfung aller Varianten wäre innerhalb des vorgegebenen Zeitrahmens nicht möglich gewesen und damit wären die bisherigen Bemühungen um eine Zulassung der Produkte in den USA hinfällig gewesen.

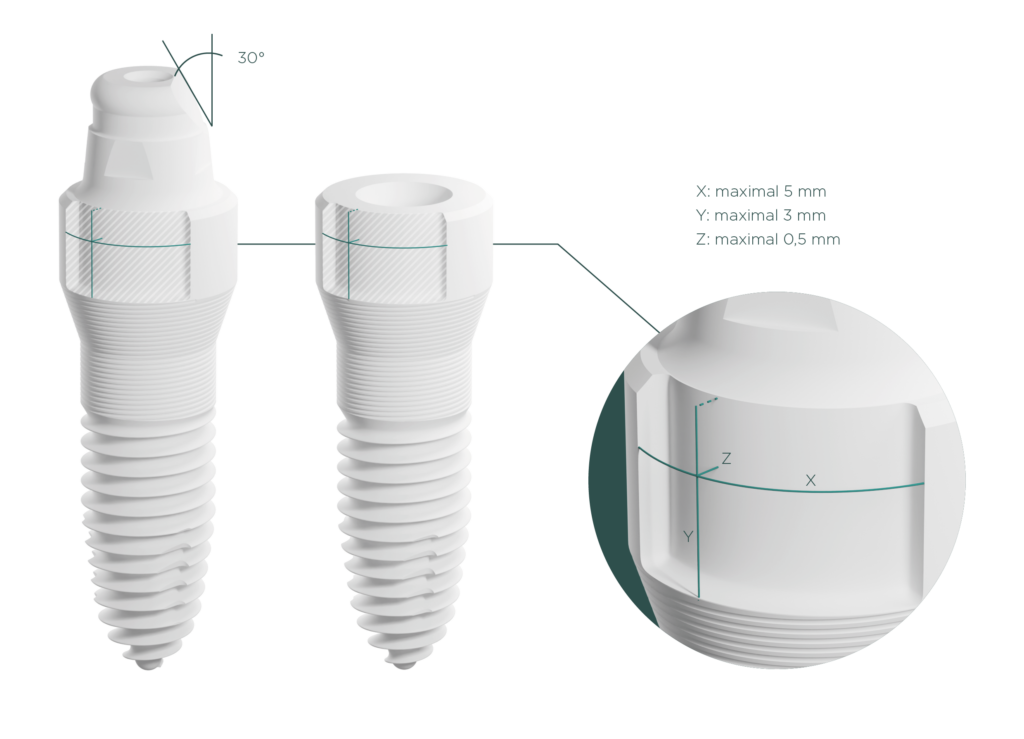
Durch die Finite-Elemente-Analyse des Ermüdungsverhaltens nach EN ISO 14801 der Varianten und der bereits erfolgreich physikalisch zugelassenen Zirkonoxidimplantate konnte eine vergleichende Analyse durchgeführt werden. Der bereits durchgeführte Versuchsaufbau wird in der FEA mit der gleichen Implantatgeometrie und den gleichen Einbettungsteilen (Prüfzylinder und halbkugelförmige Belastungskappe) nachgebildet. Anschließend wurden die Varianten mit unterschiedlichen Abutmenthöhen und den maximalen Aussparungen der beschleifbaren Implantate verglichen. Anhand der berechneten Größen wie der Vergleichsspannung (von Mises), der maximalen Hauptspannung und der Normalspannung in Z-Richtung (Biegerichtung) und anderen können die Auswirkungen der Veränderung bewertet werden.

Die Spannungsverteilung und die Höhe der Maximalwerte sind geringer und unterscheiden sich nicht signifikant von den bereits physikalisch getesteten Worst-Case-Varianten. Die Veränderung der Pfostenhöhe sowie das Beschleifen der Implantate hatten keinen signifikanten Einfluss auf die Spannungsverteilung in den kritischen Bereichen und führen daher nicht zu einer reduzierten Lebensdauer der Varianten. Die FEA-Analysen von Simq konnten nachweisen, dass die bereits physikalisch getesteten Varianten die Worst-Case-Varianten darstellen. Die Anfrage wurde erfolgreich beantwortet und damit eine unverzögerte Marktzulassung für den US-Markt sichergestellt.
Additional sources
Paper by Prof. Dr. Dr. Max Mustemann zu Mühlhausen
Written title of the paper, can also be a little longer
Überzeugen Sie sich selbst
Vereinbaren Sie jetzt Ihren persönlichen Online-Termin





